【化学基礎】物質量④〜molを中心とした単位の換算〜【授業実践備忘録】
これまで化学基礎の物質量(mol)の授業実践について投稿を続けて参りましたが、これがラストになります。
molは原子・分子・イオンが多数集まってできた"おにぎり"であって、これを基準に粒子の個数・質量・(気体の)体積などについてつなげて考えることができます。
今回の記事では、私がmolを中心とした計算問題について、普段の授業でどのように指導・説明しているかを綴って参ります。
単位の換算のフレーム
先程も綴りましたが、molは原子・分子・イオンを数多く集めてできたひとかたまりの"おにぎり"と考えることができます。
この"おにぎり"から物質をつくる粒子の個数・物質の質量・気体の体積について捉えます。

見方を変えれば、molを媒介にして、粒子の個数・質量・(気体の)体積の換算もできるということになります。
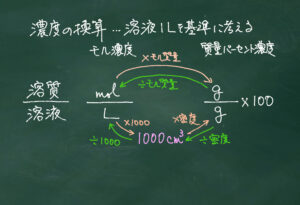
このように図を示すことで、molから他の単位に換算するときは掛け算、逆の場合は割り算を行うことと、個・g・Lの間で換算を行う場合は、スタートとゴールを定め、矢印に沿って計算すればよいことがわかります。
現在ではほとんどの教科書で下の板書のような単位換算のフレームが記されていますが、私の授業でも活用しています。
ただ、割り算については、教科書では分数式で表記されていますが、私の板書では「÷」の記号を使っています。
これは賛否両論あるやもしれませんが、生徒にとって馴染みのあるものであり、使えるものはフル活用するという考えが私にはあり、このような表記に致しました。
特に、単位の換算が分からないという生徒に対しては、普段の学習においても何度も下のフレームを書くように指示しています。
テストのときには、監督の先生から「始め」の合図が出たらすぐにこのフレームが自然に書けるようにすることを強調しています。

計算問題の指導と解説
私の授業では教科書の問題を解説する際、上に示したフレームを使い、スタートとゴールと道筋を示します。
その上で計算式を板書しています。
特に、式を示す際は単位をつけていますが、単位は数値に掛かっている文字式と同様に扱うものであり、単位をつけることによって計算の間違いを防げることを生徒には伝えています。
ただ、学力が中位〜下位の生徒には単位をつけて計算式を示すことが逆にややこしいと感じるようです。


コメント&お問い合わせ承ります
この記事に関しまして何かご意見・ご質問・ご感想などがございましたら、当社サイトの右上にありますお問い合わせフォームよりコメントをお寄せください。
皆様のコメントは、この記事をご覧になっている先生方や、私自身にとってもこれからの授業づくりに有益になるものと思います。
また、この記事をご覧になっている高校理科の先生方の中には、こんなお悩みを抱えていらっしゃいませんか?
- これまでの授業で生徒の反応が思うように得られなかった。
- これからの授業で何をどう教えたらいいのかわからない。
- 教科横断型あるいは探究的な学びを授業で取り入れたい。
そんな先生方のために、高校理科の授業づくりやスケジューリングの支援事業を行っています。
この記事に関するコメントも含め、理科の授業や、お仕事のスケジューリングなどでお悩みなどがございましたら、ぜひお話をお聴かせください。
どんな些細なことでも構いませんので、当社サイトの右上にありますお問い合わせフォームよりコメントをお寄せください。
ここまでご覧いただきありがとうございました。
文責:滝沢