【化学基礎】物質量②〜1molの質量はどう量る?〜【授業実践備忘録】
前回に引き続き、高校化学で学ぶ物質量についてまたもや投稿致します。
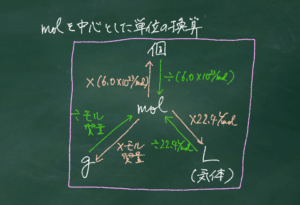
前回の投稿で、物質量(mol)=原子・分子・イオンを数多く集めてできた"おにぎり"を数える単位であると説明しました。
では、なぜmolという"おにぎり"をもとに原子・分子・イオンについて考えるのでしょうか?
それは、物質の質量や体積を人間の目に分かるようにするためです。
今回の記事では、molを使って物質の質量を考えることをテーマに綴りたいと思います。
物質1molの質量
19世紀以前、元素の質量は原子量・分子量・式量で表されていましたが、これらはあくまで"比"。
物質が実際に何gなのかを表しているわけではありません。
それでも、粒子を1mol分集めると、なんと原子量・分子量・式量にgをつけた値になってしまうのです!
この物質1molの質量はモル質量と呼びます。

なお、1molの質量=モル質量は物質の種類によって変わります。


コメント&お問い合わせ承ります
この記事に関しまして何かご意見・ご質問・ご感想などがございましたら、当社サイトの右上にありますお問い合わせフォームよりコメントをお寄せください。
皆様のコメントは、この記事をご覧になっている先生方や、私自身にとってもこれからの授業づくりに有益になるものと思います。
また、この記事をご覧になっている高校理科の先生方の中には、こんなお悩みを抱えていらっしゃいませんか?
- これまでの授業で生徒の反応が思うように得られなかった。
- これからの授業で何をどう教えたらいいのかわからない。
- 教科横断型あるいは探究的な学びを授業で取り入れたい。
そんな先生方のために、高校理科の授業づくりやスケジューリングの支援事業を行っています。
この記事に関するコメントも含め、理科の授業や、お仕事のスケジューリングなどでお悩みなどがございましたら、ぜひお話をお聴かせください。
どんな些細なことでも構いませんので、当社サイトの右上にありますお問い合わせフォームよりコメントをお寄せください。
ここまでご覧いただきありがとうございました。
文責:滝沢